Khám Phá Cấu Tạo Nguyên Tử: Hạt Nhân và Lớp Vỏ Electron
Nguyên tử, viên gạch cơ bản của mọi vật chất, không phải là một khối đặc như ta tưởng tượng mà được cấu tạo từ những hạt nhỏ hơn rất nhiều. Cụ thể, mỗi nguyên tử bao gồm hai phần chính: hạt nhân mang điện tích dương nằm ở trung tâm và lớp vỏ electron mang điện tích âm chuyển động xung quanh.
Hạt Nhân Nguyên Tử: Proton và Neutron
Hạt nhân, tuy chiếm một thể tích rất nhỏ so với toàn bộ nguyên tử, lại chứa gần như toàn bộ khối lượng của nó. Thành phần của hạt nhân bao gồm hai loại hạt chính là proton và neutron.
- Proton (p): Mang điện tích dương (+1) và có khối lượng xấp xỉ 1 đơn vị cacbon (đvC). Số proton trong hạt nhân xác định nguyên tố hóa học của nguyên tử. Ví dụ, tất cả các nguyên tử cacbon đều có 6 proton trong hạt nhân.
- Neutron (n): Không mang điện tích và có khối lượng gần bằng proton (khoảng 1 đvC). Neutron đóng vai trò quan trọng trong việc ổn định hạt nhân và tạo nên các đồng vị của một nguyên tố.
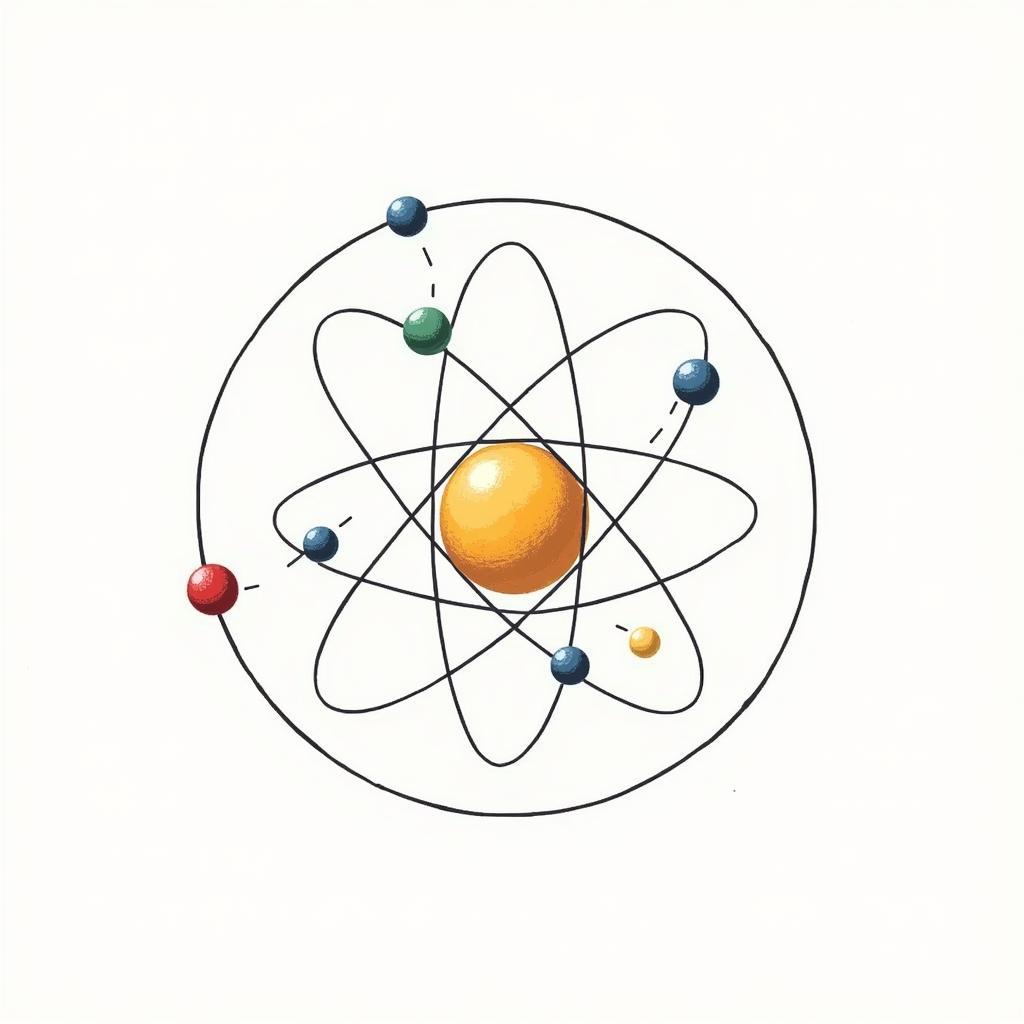 Cấu tạo nguyên tử
Cấu tạo nguyên tử
Lớp Vỏ Electron: Nơi Diễn Ra Các Liên Kết Hóa Học
Lớp vỏ electron là vùng không gian xung quanh hạt nhân, nơi các electron mang điện tích âm (-1) chuyển động không ngừng. Khối lượng của electron rất nhỏ so với proton và neutron, gần như không đáng kể.
Sự sắp xếp của các electron trong lớp vỏ tuân theo những quy tắc nhất định và quyết định tính chất hóa học của nguyên tố. Các electron ở lớp vỏ ngoài cùng, còn được gọi là electron hóa trị, đóng vai trò chủ chốt trong việc hình thành liên kết hóa học giữa các nguyên tử.
Các Loại Nguyên Tử: Đồng Vị và Ion
Ngoài cấu trúc cơ bản, nguyên tử còn tồn tại dưới các dạng khác nhau như đồng vị và ion.
Đồng Vị: Cùng Số Proton, Khác Số Neutron
Đồng vị là những nguyên tử của cùng một nguyên tố hóa học, có cùng số proton (số hiệu nguyên tử) nhưng khác số neutron trong hạt nhân. Do đó, các đồng vị của một nguyên tố có cùng tính chất hóa học nhưng khác nhau về một số tính chất vật lý như khối lượng nguyên tử.
Ví dụ: Nguyên tố cacbon có 3 đồng vị phổ biến là ¹²C, ¹³C và ¹⁴C. Cả ba đồng vị này đều có 6 proton nhưng số neutron lần lượt là 6, 7 và 8.
Ion: Khi Nguyên Tử Nhận hoặc Nhường Electron
Ion là những nguyên tử hoặc nhóm nguyên tử mang điện tích. Khi một nguyên tử nhận thêm electron, nó sẽ mang điện tích âm và được gọi là ion âm (anion). Ngược lại, khi một nguyên tử mất đi electron, nó sẽ mang điện tích dương và được gọi là ion dương (cation).
Ví dụ: Nguyên tử natri (Na) có xu hướng mất đi 1 electron để trở thành ion natri (Na⁺), trong khi nguyên tử clo (Cl) có xu hướng nhận thêm 1 electron để trở thành ion clorua (Cl⁻).
 Đồng vị và ion
Đồng vị và ion
Bài Tập Vận Dụng Kiến Thức Cấu Tạo Nguyên Tử
Để củng cố kiến thức về cấu tạo nguyên tử, các em có thể tham khảo một số bài tập vận dụng sau đây:
- Xác định số proton, neutron và electron của các nguyên tử và ion sau: ¹⁶O, ¹⁹F⁻, ²⁴Mg²⁺, ³⁵Cl.
- Cho biết số hiệu nguyên tử, số khối và kí hiệu nguyên tử của nguyên tố X, biết nguyên tử X có 12 proton và 13 neutron.
- Nguyên tố Y có hai đồng vị là ⁵⁴Y và ⁵⁶Y. Biết đồng vị ⁵⁶Y chiếm 90% số nguyên tử Y trong tự nhiên. Tính nguyên tử khối trung bình của Y.
Kết Luận
Hiểu rõ về Giải Bài Tập Hóa 10 Bài 4 và cấu tạo nguyên tử là chìa khóa để mở ra cánh cửa vào thế giới hóa học đầy thú vị. Nắm vững kiến thức này sẽ giúp các em học sinh tự tin hơn trong việc giải quyết các bài tập hóa học và tiếp thu những kiến thức phức tạp hơn trong tương lai.
Câu hỏi thường gặp
1. Proton và neutron khác nhau như thế nào?
Trả lời: Proton mang điện tích dương (+1) trong khi neutron không mang điện tích.
2. Số electron trong nguyên tử trung hòa về điện được xác định như thế nào?
Trả lời: Trong nguyên tử trung hòa về điện, số electron bằng số proton.
3. Tại sao electron lại chuyển động xung quanh hạt nhân?
Trả lời: Do lực hút tĩnh điện giữa hạt nhân mang điện tích dương và electron mang điện tích âm.
4. Đồng vị có ảnh hưởng gì đến tính chất của nguyên tố?
Trả lời: Đồng vị có ảnh hưởng đến một số tính chất vật lý của nguyên tố như khối lượng nguyên tử, nhưng không ảnh hưởng đến tính chất hóa học.
 Liên kết hóa học
Liên kết hóa học
5. Ion được hình thành như thế nào?
Trả lời: Ion được hình thành khi một nguyên tử nhận thêm hoặc mất đi electron.
Tìm hiểu thêm về:
Hãy liên hệ với chúng tôi theo số điện thoại 02033846993, email giaibongda@gmail.com hoặc địa chỉ X2FW+GGM, Cái Lân, Bãi Cháy, Hạ Long, Quảng Ninh, Việt Nam để được hỗ trợ 24/7.
