Nhiệt hóa học là một nhánh quan trọng trong hóa học, nghiên cứu về nhiệt năng hấp thụ hoặc giải phóng trong các phản ứng hóa học. Bài viết này cung cấp cho bạn những kiến thức cơ bản về Bài Tập Nhiệt Hóa Học Có Lời Giải, giúp bạn tự tin chinh phục mọi kỳ thi.
Nhiệt Hóa Học Là Gì?
Nhiệt hóa học là ngành hóa học nghiên cứu sự thay đổi năng lượng liên quan đến các quá trình hóa học và vật lý. Đây là một phần quan trọng trong hóa học, giúp bạn hiểu rõ hơn về bản chất của phản ứng và dự đoán khả năng xảy ra của chúng.
Các Khái Niệm Cơ Bản Trong Nhiệt Hóa Học
Để giải quyết bài tập nhiệt hóa học, bạn cần nắm vững một số khái niệm cơ bản sau:
- Nhiệt phản ứng (ΔH): Lượng nhiệt được hấp thụ hoặc giải phóng trong một phản ứng hóa học ở điều kiện áp suất không đổi.
- Phản ứng tỏa nhiệt: Phản ứng giải phóng nhiệt ra môi trường xung quanh (ΔH < 0).
- Phản ứng thu nhiệt: Phản ứng hấp thụ nhiệt từ môi trường xung quanh (ΔH > 0).
- Entanpi (H): Hàm trạng thái của hệ nhiệt động lực học, biểu thị tổng năng lượng bên trong của hệ ở điều kiện áp suất không đổi.
- Định luật Hess: Tổng entanpi của một phản ứng hóa học không phụ thuộc vào con đường phản ứng, mà chỉ phụ thuộc vào trạng thái ban đầu và trạng thái cuối cùng của hệ.
Các Loại Bài Tập Nhiệt Hóa Học Thường Gặp
Dưới đây là một số dạng bài tập nhiệt hóa học phổ biến:
1. Tính Nhiệt Phản Ứng (ΔH)
Ví dụ: Tính ΔH của phản ứng sau, biết năng lượng liên kết của các chất như sau:
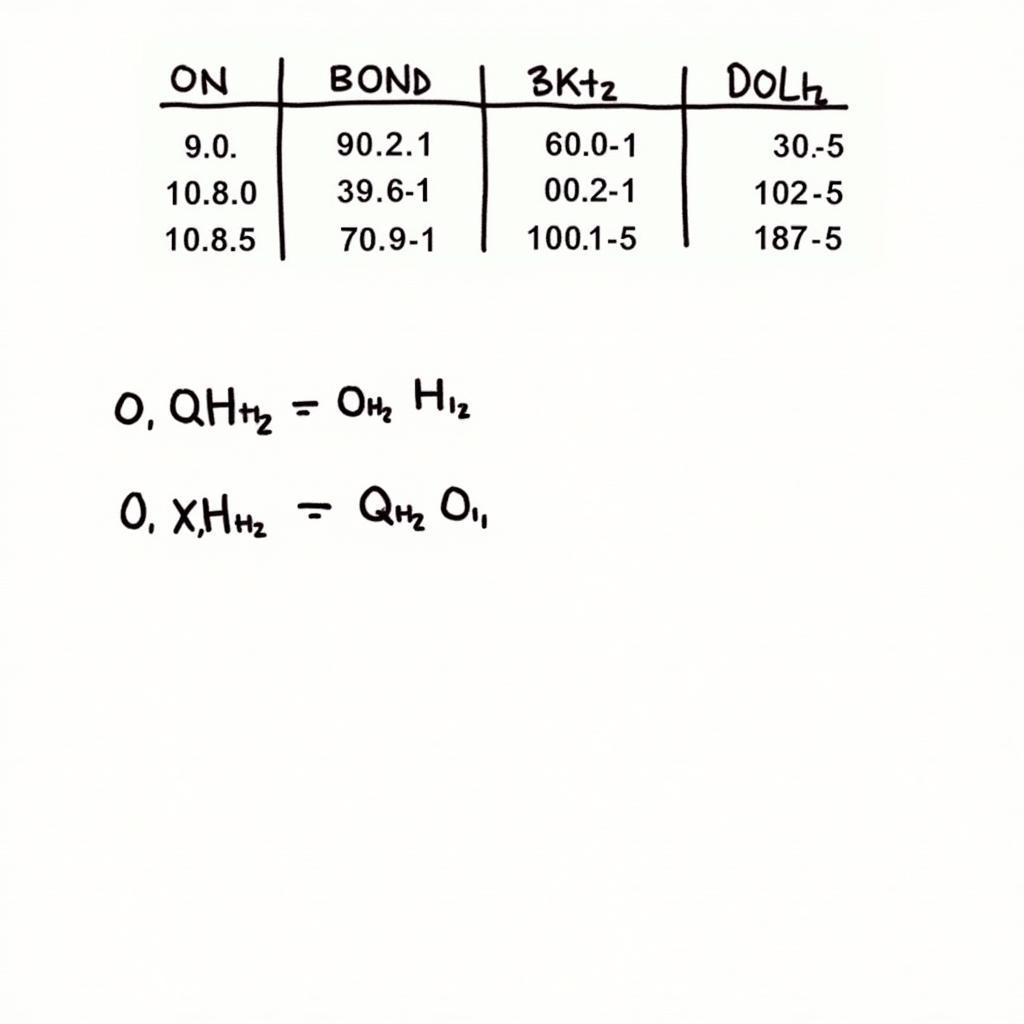 Tính nhiệt phản ứng
Tính nhiệt phản ứng
Lời giải:
Để tính ΔH, ta sử dụng công thức:
ΔH = Σ (Năng lượng liên kết của các chất phản ứng) – Σ (Năng lượng liên kết của các chất sản phẩm)
Lưu ý:
- Năng lượng liên kết luôn là số dương.
- Đơn vị của ΔH thường là kJ/mol.
2. Áp Dụng Định Luật Hess
Ví dụ: Tính ΔH của phản ứng sau, sử dụng thông tin từ các phản ứng đã cho:
Lời giải:
Để áp dụng định luật Hess, ta cần thực hiện các bước sau:
- Bước 1: Xác định phản ứng cần tính ΔH.
- Bước 2: Tìm các phản ứng đã cho có chứa các chất trong phản ứng cần tính.
- Bước 3: Điều chỉnh hệ số và đảo ngược phản ứng (nếu cần) để các chất trong phản ứng cần tính xuất hiện ở đúng vị trí.
- Bước 4: Cộng các phản ứng đã điều chỉnh và ΔH tương ứng để thu được ΔH của phản ứng cần tính.
3. Tính Hiệu Suất Phản Ứng Dựa Trên Nhiệt
Ví dụ: Cho phản ứng sau, biết ΔH = -100 kJ/mol. Tính khối lượng 40 giải phóng cần dùng để thu được 50 kJ nhiệt?
Lời giải:
Để tính khối lượng chất phản ứng, ta cần thực hiện các bước sau:
- Bước 1: Tính số mol chất phản ứng dựa trên ΔH và lượng nhiệt đã cho.
- Bước 2: Tính khối lượng chất phản ứng dựa trên số mol và khối lượng mol.
Mẹo Giải Bài Tập Nhiệt Hóa Học Hiệu Quả
Dưới đây là một số mẹo giúp bạn giải bài tập nhiệt hóa học hiệu quả:
- Nắm vững lý thuyết: Đảm bảo bạn hiểu rõ các khái niệm cơ bản, định luật và công thức liên quan đến nhiệt hóa học.
- Luyện tập thường xuyên: Giải nhiều bài tập từ cơ bản đến nâng cao để nâng cao kỹ năng tính toán và áp dụng kiến thức.
- Rèn luyện tư duy logic: Phân tích đề bài kỹ lưỡng, xác định thông tin đã cho và thông tin cần tìm.
- Sử dụng sơ đồ: Vẽ sơ đồ phản ứng và ghi chú các giá trị ΔH có thể giúp bạn hình dung và giải quyết bài toán dễ dàng hơn.
- Kiểm tra lại kết quả: Luôn kiểm tra lại kết quả sau khi tính toán để đảm bảo độ chính xác.
Kết Luận
Bài viết đã cung cấp cho bạn những kiến thức cơ bản về bài tập nhiệt hóa học có lời giải. Hy vọng những thông tin này sẽ giúp bạn tự tin hơn trong việc học tập và chinh phục môn hóa học.
Cần hỗ trợ? Hãy liên hệ Số Điện Thoại: 02033846993, Email: [email protected] Hoặc đến địa chỉ: X2FW+GGM, Cái Lân, Bãi Cháy, Hạ Long, Quảng Ninh, Việt Nam. Chúng tôi có đội ngũ chăm sóc khách hàng 24/7.
